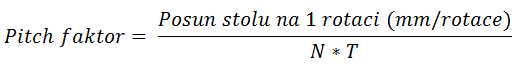Napětí rentgenky
Napětí rentgenky je rozdíl elektrických potenciálů mezi anodou a katodou rentgenky, tj. napětí, kterým jsou urychlovány elektrony vyletující z katody. Napětí rentgenky určuje maximální energii fotonů v rentgenovém (rtg) spektru, energetickou distribuci rtg spektra a taktéž celkový výstup z rentgenky. Typicky jsou při CT skenování používány hodnoty napětí v rozmezí 80-140 kV. Napětí ovlivňuje i střední energii spektra, která pak ovlivňuje lineární součinitele zeslabení. Změna napětí vede ke změně absorpce v jednotlivých materiálech, což má vliv na kontrast, šum a dávku pacientovi. Obecně platí, že fotony vyšší energie mají menší pravděpodobnost interakce, mají větší penetraci. U nižších energií mají materiály (zvláště jód) vyšší lineární součinitel zeslabení (více fotonů se absorbuje v pacientovi), proto se při nižších energiích dramaticky zlepšuje kontrast obrazu. Nicméně to znamená vyšší dávku pacientovi, proto je pro dostatečnou dávku na výstupu pacienta nutné zvýšit dávku na vstupu pacienta.
Při uvážení snížení kV je nutné vzít v potaz taktéž velikost pacienta. Pro objemově velké pacienty není možné použít příliš nízkou hodnotu kV, protože pak fotony nemají dostatečnou penetraci a pro získání určité hodnoty poměru signál/šum tím neúměrně narůstá dávka pacientovi. Naopak pro malé pacienty jsou dostatečné i fotony o nižší penetraci, proto lze s výhodou použít nižší hodnotu kV, např. 100 kV nebo 80 kV, čímž se výrazně zlepšuje kontrast v obraze, zvláště pak kontrast jodové kontrastní látky. Proto lze také snížit celkové množství fotonů, a tím i dávku pacientovi. Při nižší hodnotě kV se liší výsledná CT čísla (Hounsfieldovy jednotky) v jednotlivých tkáních od CT čísel při standardních 120 kV, což může způsobit nepříjemnost např. v případech, kdy je použit bolus tracking.
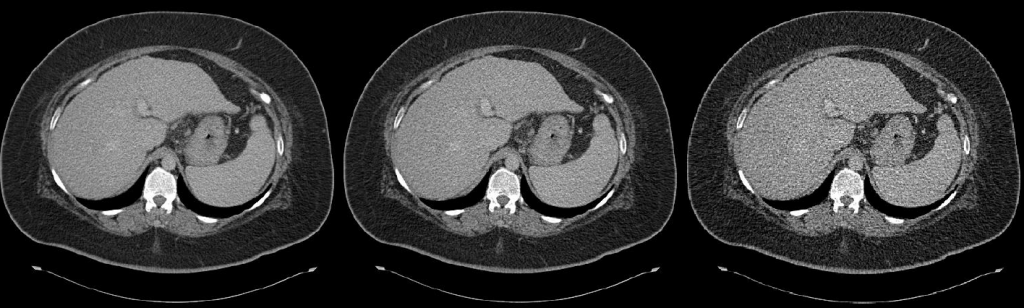
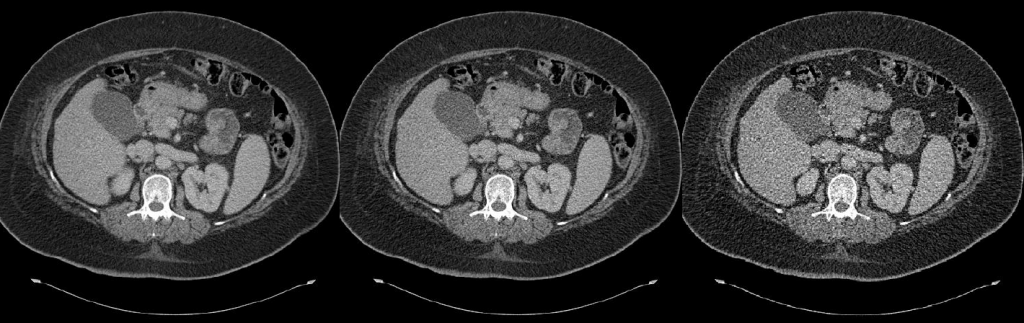
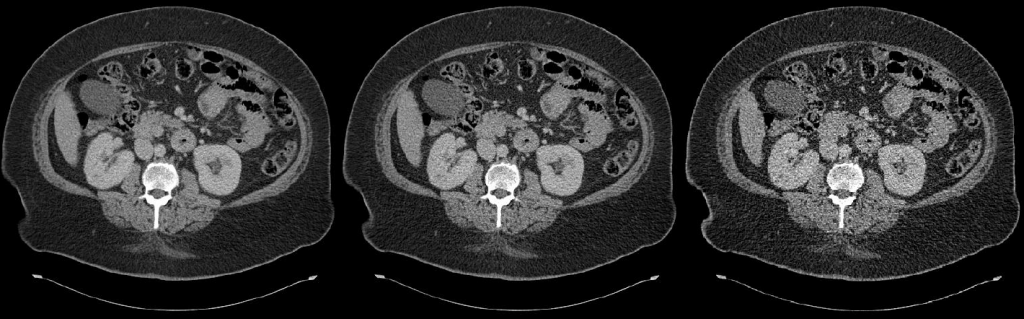
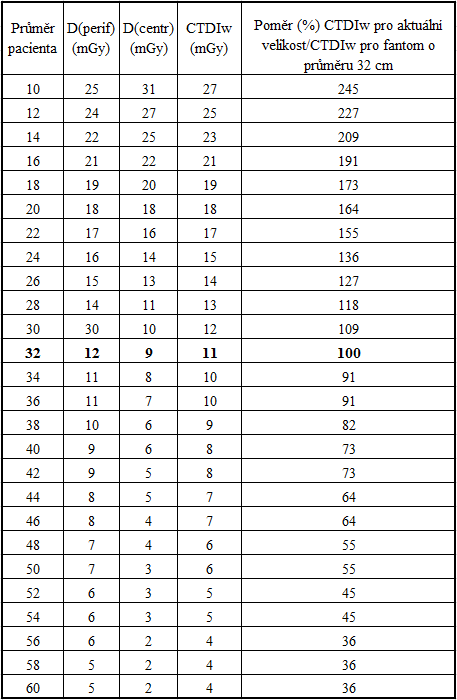
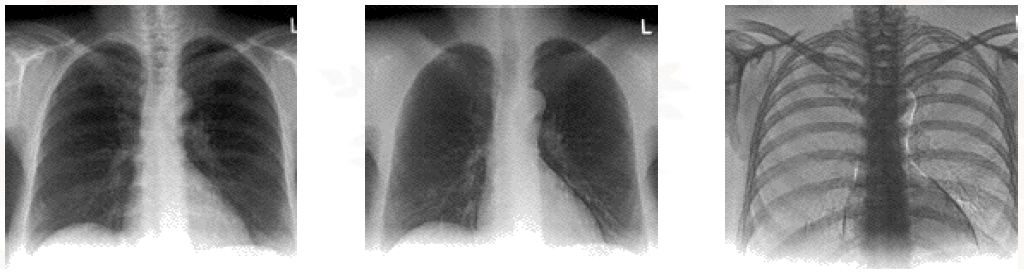
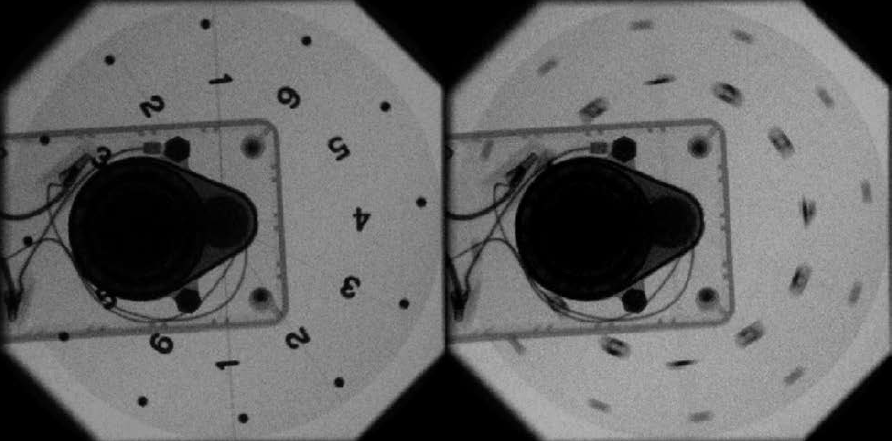
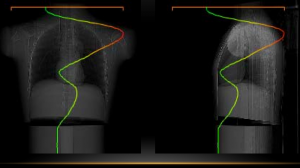
Ukázka kontrastu v obraze společně s dávkou a hodnotou CT čísel v závislosti na napětí rentgenky je uvedena na obr. 1.
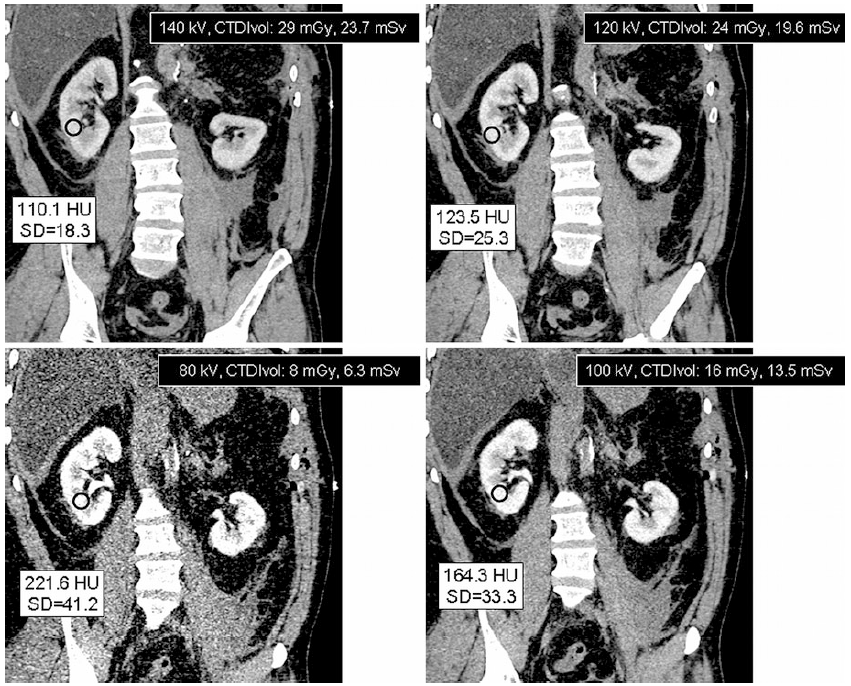 Obr. 1: Ukázka CT obrazů v závislosti na různé hodnotě použitých kV [2]
Obr. 1: Ukázka CT obrazů v závislosti na různé hodnotě použitých kV [2]
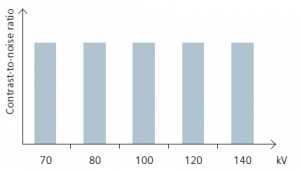
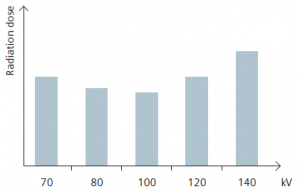
Na obr. 2 je uvedena ukázka kontrastu pro různá napětí a taktéž pro různé rozměry eliptického fantomu simulujícího různé velikosti pacienta.
 Obr. 2: Kontrast a šum v obraze pro různé hodnoty napětí a různé velikosti fantomu
Obr. 2: Kontrast a šum v obraze pro různé hodnoty napětí a různé velikosti fantomu
Použitá literatura:
[1] Wolbarst AB, Capasso P, Godfrey DJ, Price RR, Whiting BR, Hendee WR. Advances in Medical Physics 2012. Volume 4. Medical Physics Publishing, 2012
[2] Tack D, Kalra MK, Gevenois PA. Radiation Dose from Multidetector CT. Second Edition. Springer, 2012
Další články:
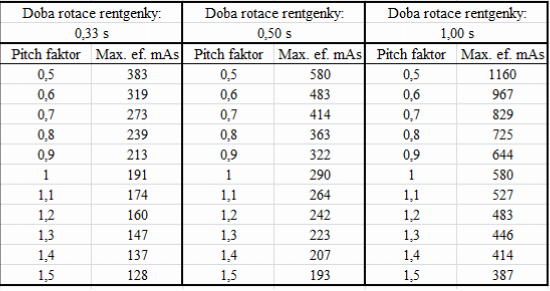
1) Doba rotace rentgenky, proud rentgenky
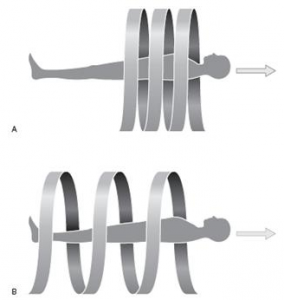
2) Pitch faktor a ukázka interakce pitch faktoru a dalších parametrů
3) Tloušťka rekonstruovaného řezu
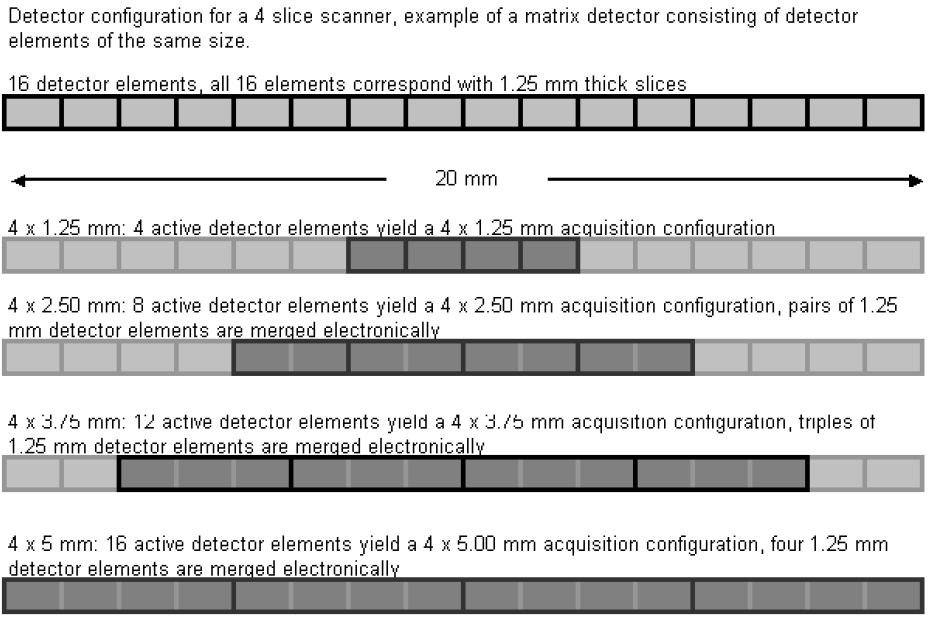
4) Konfigurace detektoru
5) Napětí rentgenky
6) Rekonstrukční kernel/algoritmus